À la différence de ce que la science-fiction pourrait nous faire croire, les nanobots ne sont pas des robots mécaniques à l’échelle nanométrique. Dans le monde réel, la nanotechnologie robotique consiste à programmer des molécules pour effectuer des tâches spécifiques.
Les nanobots ne sont pas les robots miniatures de la science-fiction, mais des molécules programmables qui redessinent déjà la médecine.
_La réalité : pas de robots mécaniques, mais des molécules et cellules programmées pour cibler les maladies au niveau cellulaire.
_La promesse médicale : médicaments ultra-ciblés, diagnostic précoce du cancer et régénération de la moelle épinière — avec des résultats précliniques spectaculaires.
_Le frein : aucun essai clinique de phase 1 validé en 2026, la fabrication à grande échelle et la biocompatibilité restent des verrous majeurs.
Le domaine des nanotechnologies gagne du terrain. Le marché mondial des nanorobots est évalué à 7,486 milliards USD en 2025. Il devrait atteindre 15,015 milliards USD d’ici 2030, selon Research and Markets. Mais que sont vraiment les nanobots ? Voici un guide pour comprendre leurs réelles avancées.
Qu’appelle-t-on nanobots ?
Dans le terme nanobot, nous pouvons distinguer deux éléments : nano- et bot. À première vue, cela pourrait faire croire qu’il s’agit de robots à l’échelle nanométrique. Cependant, ce n’est pas réellement le cas. La nanotechnologie robotique fait référence à des nanoparticules qui mesurent de 1 à 100 nanomètres. Pour vous donner une idée plus précise, les nanobots peuvent être 1,4 million de fois plus petit petits que la largeur du cerveau.
Pour rappel, les robots sont des dispositifs autonomes destinés à effectuer des tâches précises. Les nanobots peuvent donc correspondre à des nanomoteurs, des nanoactionneurs ou encore des nanocapteurs. Par ailleurs, en équivalence à la manipulation d’objets chez les robots ordinaires, les nanorobots assemblent des pièces de taille nanométrique, manipulent des cellules ou des molécules biologiques.
La théorie de la nanotechnologie
Le concept de la nanotechnologie remonte à 1959, quand le physicien Richard Feynman a prononcé un discours intitulé « There’s Plenty of Room at the Bottom ». Sa théorie évoquait des machines miniaturisées et un encodage de données dans des espaces minuscules.
Puis, en 1986, K. Eric Drexler a publié le livre Engines of Creation : The Coming Era of Nanotechnologyprésentant l’idée de nanodispositifs programmables et autoreproductibles. Sur le plan pratique, les nanobots peuvent donc construire et manipuler des objets à l’échelle moléculaireet avec une grande précision.
À quoi servent les nanobots ?
Rappelons encore une fois que les nanobots ont une taille comparable à celle des cellules biologiques. Pour Drexler, étant donné que ces dispositifs opèrent à l’échelle atomique, ils pourraient être utilisés pour construire ou démonter tout type de matériaux. Cette capacité permettrait par exemple d’assainir l’environnement en le débarrassant des particules nocives.
Mais actuellement, le fait que les nanorobots sont référencés comme des molécules programmables intéresse surtout les chercheurs dans le domaine de la médecine.
Le marché des nanobots reste émergent et dépend fortement de la recherche académique. En revanche, il s’inscrit dans une dynamique plus large de croissance rapide de la nanomédecine et des micro-/nano-dispositifs intelligents , qui constituent aujourd’hui le principal moteur économique du secteur.
Les projections à l’horizon 2030-2033 anticipent une montée en puissance progressive des technologies inspirées de la nanorobotique, en particulier dans les domaines suivants :
- Administration ciblée de médicaments, via des nanoparticules intelligentes, des nano-vecteurs stimuli-réactifs ou des micro-robots guidés par champs externes
- Médecine personnalisée, avec des systèmes capables d’adapter leur action à l’environnement biologique du patient
- Diagnostic avancé et imagerie moléculaire, grâce à des nano-dispositifs détectant des biomarqueurs à très faible concentration
Comment les nanobots sont-ils utilisés en médecine ?
En termes simples, le rôle des nanobots en médecine consiste à délivrer des médicaments aux cellules malades ou à neutraliser les toxines. Par exemple, la nanotechnologie offre une voie vers le diagnostic précoce du cancer. En effet, les scientifiques ont mis au point des nanobots qui peuvent mesurer les biomarqueurs, même à faibles concentrations, avec précision.
Il existe différentes approches nanotechnologiques explorées dans ce domaine.
Les nanomoteurs autopropulsés
Les nanobots en question ne contiennent aucun matériau biologique et peuvent utiliser des champs magnétiques, ultrasonores ou lumineux comme actionneurs. Ces robots de nanotechnologies peuvent par exemple être programmés pour transporter des charges utiles moléculaires. Cela peut être une solution thérapeutique pour traiter une maladie.
Les nanobots de type cellulaire
C’est ce deuxième type de nanorobots qui est utilisé pour éliminer les bactéries et les toxinesdu sang. Ils se composent de nanofils d’or recouvert de membranes hybrides de plaquettes et de globules rouges.
Les plaquettes fixent les agents pathogènes tandis que les globules rouges absorbent et neutralisent les toxines que les bactéries produisent. Un autre type de nanobots dit biohybrides proviennent d’organismes biologiques tels que les cellules minimisées, l’ADN, etc.
Les robots vivants
Certains chercheurs développent des formes de vie synthétiquesà partir de cellules biologiques. Par exemple, des scientifiques de l’université de Vermont ont crée les xénobots à partir de cellules souches de grenouilles. Ces derniers sont capables de se déplacer, d’effectuer différentes tâches comme la guérison et l’auto-guérison et peuvent même se reproduire.
L’origami d’ADN
Cette approche consiste à construire des ADN biosynthétiques en s’inspirant de la nature. Les nanobots ADN, comme ils sont appelés, correspondent à des origamis d’ADN. Autrement dit, les molécules sont pliées suivant une configuration géométrique complexe en 3D.
Entre autres, le développement des robots ADN permettrait de détruire les cellules cancéreuses. Pour ce faire, ils se déplaceraient dans le sang pour délivrer des substances coagulantes au niveau de l’irrigation de la tumeur. Cela permettrait alors de couper son alimentation en sang et, par conséquent, d’empêcher sa croissance, voire la tuer.
Nanomoteurs hybrides magnétiques / électriques
Des microrobots Janus métallo‑diélectriques combinent aujourd’hui des mécanismes d’action à la fois magnétiques et électriques. Ils proposent un contrôle de mouvement 3D beaucoup plus fin. Par exemple, des études de 2025 démontrent qu’ils peuvent effectuer des trajectoires « hors plan » (transition 2,5D) grâce à la lévitation magnétique et à des pièges électrostatiques.
Cette technologie ouvre des possibilités pour des interventions localisées, telles que l’administration ciblée de médicaments ou la manipulation de cellules vivantes dans des structures en 3D.
Le tournant des essais cliniques sur l’homme
Une rupture majeure se profile. D’importants travaux précliniques ont démontré le potentiel des nanobots. En janvier 2024, une équipe dirigée par Samuel Sánchez (IBEC) a réduit des tumeurs de la vessie de 90 % chez la souris. Elle a utilisé des nanorobots auto-propulsés. Cette technologie, nommée MotionTx, a été présentée au Mobile World Congress 2026 à Barcelone. Le roi Felipe VI d’Espagne a visité le stand de la start-up.
En parallèle, des chercheurs chinois ont développé des nanobots à base de peptides pour le cancer colorectal.
Cette avancée utilise des nanorobots qui reconnaissent la protéine PD-L1. Dans des modèles animaux, ces nanobots ont montré une efficacité supérieure au protocole combiné αPD-L1+oxaliplatine.
C’est un traitement de référence. Aucun essai clinique de phase 1 n’a encore été annoncé à ce jour. Plusieurs équipes, dont celle de l’IBEC, poursuivent activement leurs travaux précliniques.
Défis et enjeux des essais cliniques des nanobots
Malgré des résultats précliniques prometteurs, l’intégration des nanobots en médecine rencontre des défis majeurs.
Premièrement, la fabrication à grande échelle s’annonce bien plus complexe. Effectivement, chaque nanobot doit respecter des critères stricts de taille, de stabilité et de fonctionnalisation. Sans cela, ils ne seront pas en mesure de transporter des agents thérapeutiques.
Ensuite, la sécurité et la biocompatibilité s’alignent au centre des préoccupations. Aujourd’hui, les autorités de santé exigent des preuves solides sur l’innocuité des nanobots. Même requête à propos de leur dégradation dans le corps et de l’absence d’effets secondaires à long terme.
Ensuite, sur le plan réglementaire et éthique, des questions se posent sur la surveillance des dispositifs et le consentement des patients. Enfin, il va falloir démontrer l’efficacité clinique dans des essais rigoureux. Ceci, afin de garantir que ces nanorobots délivrent les traitements de manière précise et fiable.
Ces enjeux soulignent que la route vers une adoption clinique généralisée est effectivement semée d’embûches. Toutefois, chaque étape franchie rapproche les nanobots d’une utilisation médicale révolutionnaire.
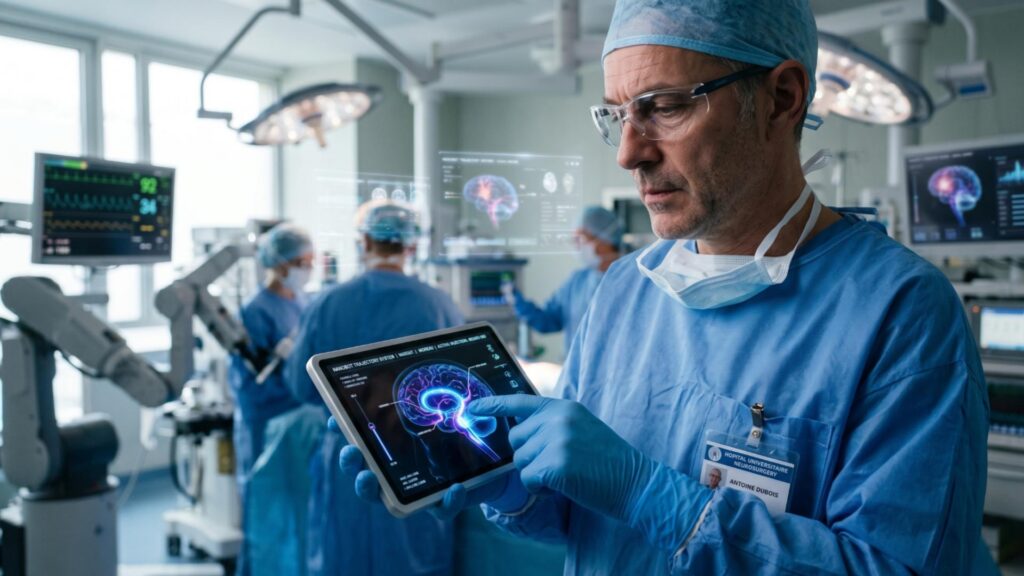
Des micro-robots font remarcher des souris paralysées.
Des chercheurs de l’ETH Zurich ont récemment dévoilé une prouesse mondiale. Ils ont conçu des NPCbots, des micro-robots guidés par des champs magnétiques. Ces robots délivrent des cellules souches neurales directement dans la moelle épinière lésée.
Combiné à une stimulation magnéto-électrique, le traitement a restauré une quasi-intégralité des fonctions motrices chez le poisson zèbre en trois jours. Chez la souris, une amélioration notable a été observée en quatre semaines. Cette approche ouvre des possibilités inédites pour traiter les paralysies chez l’humain.
FAQ : Tout savoir sur les nanobots
Un nanobot est un dispositif programmable à l’échelle nanométrique, soit un milliardième de mètre. Il manipule des molécules ou des cellules. Contrairement aux robots de science-fiction, il n’est pas mécanique. On le conçoit à partir de matériaux biologiques, chimiques ou synthétiques.
La recherche sur les nanobots s’intensifie. Ils servent surtout à délivrer des médicaments au plus près des cellules malades. Des essais précliniques montrent leur efficacité contre les tumeurs de la vessie ou le cancer colorectal. D’autres types aident à régénérer la moelle épinière après une lésion.
Parmi les avancées marquantes, on trouve les nanomoteurs auto-propulsés à l’urée, les nanobots à peptides qui percent les membranes des cellules, et les micro-robots magnéto-électriques pour la régénération neuronale.
La FDA n’a pas encore autorisé d’essai de phase 1 pour des nanobots ciblant le cerveau. De nombreuses équipes, dont celle de l’IBEC (Barcelone), ont finalisé des études précliniques prometteuses. L’Europe est très active, avec des conférences comme Nanotech France 2026 à Paris ou l’ETPN à Dublin.
La fabrication à grande échelle reste complexe. Chaque nanobot doit respecter des critères stricts de taille, de stabilité et de fonctionnalisation. La sécurité et la biocompatibilité sont au cœur des préoccupations. Les autorités exigent des preuves sur leur dégradation dans le corps.
- Partager l'article :




Calme